上海2024年9月19日 /美通社/ -- 2024年9月17日,波士顿科学(纽约证券交易所代码:BSX)获得美国食品药品监督管理局(FDA)的批准,扩大当前一代INGEVITY™+植入式心脏起搏电极导线(放置在心脏内并连接到植入式设备的细导线)的适应证,包括与单腔或双腔起搏器连接时,对左束支区域(LBBA)进行传导系统起搏(CSP)和感知。
LBBA起搏是传统右心室起搏治疗有症状心动过缓(即心跳过慢)的替代方法。该术式是将导线放置在心脏传导系统的左束支区域(LBBA),利用心脏自身电传导系统进行起搏。该技术可以促进更好的心室同步性,并降低与传统右心室起搏相关的心力衰竭的长期风险。[1]
波士顿科学心脏节律管理与诊断部门高级副总裁兼总裁Scott Olson表示:"该适应证的批准使我们能为医生提供更多专用于LBBA的工具和教育资源,同时加强了我们对开发安全有效起搏技术的保证。我们相信,INGEVITY+植入式心脏起搏电极导线的扩大适应证将增强医生的植入体验,并将这项技术带给越来越多可以从LBBA起搏中受益的患者。"
提交给FDA用以支持扩大适应证的临床证据包括了约400名患者的INSIGHT-LBBA研究数据。该研究分析了先前因抗心动过缓起搏适应证在LBBA植入INGEVITY+植入式心脏起搏电极导线的患者,并补充了台架测试和LATITUDE™程控系统数据。
波士顿科学高级副总裁兼全球首席医疗官Kenneth Stein博士表示:"此次扩大的适应证为使用INGEVITY+植入式心脏起搏电极导线的医生提供了更多选择,使他们能够根据患者个体特征确定最合适的起搏方案。数据表明,INGEVITY+植入式心脏起搏电极导线对LBBA起搏是安全有效的。作为快速增长的起搏技术,LBBA起搏使我们能够在经过验证的导线上提供新的治疗选择,进一步提高患者的获益质量。"
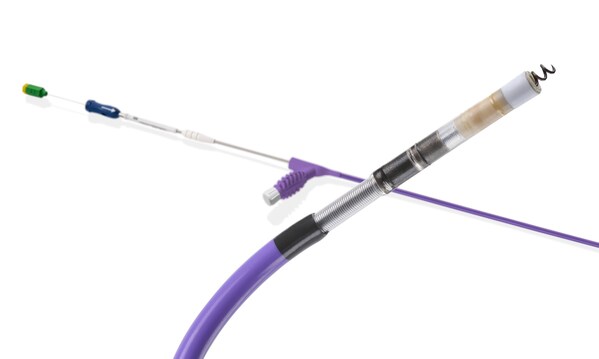
INGEVITY+植入式心脏起搏电极导线在导线放置过程中由塑性钢丝引导,钢丝可以将器械定位到心脏内的所需位置,并允许连续起搏和阻抗监测,这是有助于合理放置和固定的关键性能。在波士顿科学公司推出CSP产品组合(包括OneLINK™分屏电缆、INGEVITY+螺旋锁定工具和位点选择性起搏传送导管)之后,扩大的适应证旨在支持INGEVITY+植入式心脏起搏电极导线在LBBA中安全有效地放置。INGEVITY+植入式心脏起搏电极导线于2019年获得FDA批准,用于配合起搏器和除颤器使用。
有关INGEVITY+植入式心脏起搏电极导线的更多信息,请访问此处。
*该产品的扩大适应证尚未在中国内地获批
版权声明
广深在线内容如无特殊说明,内容均来自于用户投稿,如遇版权或内容投诉,请联系我们。